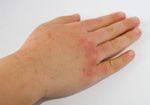
洗い流さない「手の除菌剤」は安全か?(shutterstock.com)
最近では病院に限らずスーパーなどでも、入口付近に「手の除菌剤」を常備している施設は少なくない。では、あのての除菌剤の「安全性」について、多少なりとも意識したことはあるだろうか?
実は先ごろ、米国食品医薬局(FDA)が、除菌剤や関連商品の製造元に対して、従来以上の「安全性の確認」を要求しているのだ。
洗い流さないから尿に出る!?
FDAが要求したのは、各製品のラベルに表示された有効成分が「実際に細菌を減らすかどうか」、また、それらが「長期的に無害かどうか」を示すデータの提供である。とりわけ懸念されているのは、「妊婦や小児に対する長期的影響」という点である。
ただしFDA当局は、対象製品らの「無効性」や「危険性」を勘ぐっているわけではないとも強調している。
今回の要請が出された直接のきっかけは、専門家陣で構成される独立諮問委員会の勧告を受けてのものだった。というのも、最近の研究で、除菌剤の製品消費者の尿中における「殺菌成分の濃度」が、想定よりも高めであることが判明したからだ。
これらの除菌剤は「洗い流さない(で済む)」のが利点でもあるが、それゆえ吸収力に関する安全性の疑問が浮上したようだ。
FDA医薬品評価センター(CDER)のJanet Woodcock氏は、「皆さんに広く使われている、こうした除菌系の製品は、水や石鹸が使えない時や環境においては確かに便利です。だからこそ消費者がより安心して使えるよう、その安全性と有効性を確認することが私たちの責任です」と今回の要請の意義をについてコメント。
製造会社側に追加データを要求する規則案に関しては、180日間のパブリックコメント(意見・情報・改善案)が公募されている。製造元が現行製品の販売継続を希望する場合、1年以内に該当品の新たなデータを提出しなければならなくなるようだ。
今回の要請に対して、業界団体である米国洗浄剤協会(ACI)側は、「正直、FDAは通常時の安全性や有効性を確認する過程で、すでに十分なデータを入手していると、われわれは考えておりますが……」と多少なりとも不服気味な見解を示しながらも、立場上は「完全な情報の提供に努める」と談話している。